- TOP
- >
- 大塚製薬から新薬、欧州医薬品委員会が承認推奨
新着ニュース30件
2013年11月28日 19:00
多剤耐性結核治療へ新たな一歩
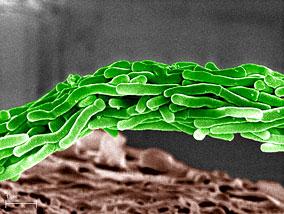
大塚製薬は11月25日、現在開発中の結核治療薬、「デラマニド」が欧州医薬品庁の医薬品委員会から販売承認の推奨を得たことを発表した。来年初旬には、欧州委員会が販売承認について最終決定を行う。正式に承認されれば、欧州では約40年ぶりの新しい結核治療薬となる。(画像は大塚製薬ニュースリリースより)
薬が効かない「多剤耐性結核」
近年、複数の1次選択薬が効かない「多剤耐性結核(MDR-TB)」が急増している。さらに、複数の2次選択薬も効かない「超多剤耐性結核(XDR-TB)」も増えている。MDR-TBの推定患者数は45万人、年間死者数は約17万人と言われており、世界的に問題となっている疾病だ。従来の治療では、治療薬の毒性が高い、治療期間が長く高額な費用がかかる、治癒率が低いなど、多くの問題がある。そのため治療できずにいる患者も多い。
デラマニドとは
本剤は、結核菌の細胞壁に含まれるミコール酸の生成を阻害することで抗菌効果を示す。多剤耐性結核の患者に対する臨床試験では、本剤を投与して結核菌の消失が認められた患者は、プラセボ群よりも53%多かった。多剤耐性結核および超多剤耐性結核の標準治療との併用療法として、効果が期待されている。現在は第3相臨床試験中で、今後さらに小児・乳児への応用のための試験も進める予定だ。
大塚製薬2013年ニュースリリース
http://www.otsuka.co.jp/company/release/2013/1125_02.html
-->