- TOP
- >
- 白血病治療薬として「ポナチニブ」を国内製造販売承認申請
新着ニュース30件
2016年1月11日 02:00
国内初
大塚製薬株式会社(以下、「大塚製薬」)は2016年1月8日、既存のチロシンキナーゼ阻害薬に抵抗性又は不耐容の慢性骨髄性白血病、フィラデルフィア染色体陽性急性リンパ性白血病の治療薬である「ポナチニブ(海外製品名:Iclusig、アイクルシグ)」について、日本国内での製造販売承認申請したことを発表した。「ポナチニブ」は、米国アリアド社が開発したチロシンキナーゼ阻害薬(以下「TKI」)で、慢性骨髄性白血病(以下「CML」)とフィラデルフィア染色体(以下「Ph」)陽性急性リンパ性白血病(以下「Ph+ ALL」)に対する新規経口治療薬として国内で初の申請となる。
CML とPh+ ALL の発症と治療
CMLの国内患者数は約11,000人と推定されており、TKI治療の進歩により死亡率は低下しているが、高齢者の人口増加に伴い患者数は増加傾向にある。急性転化期になると貧血、出血傾向、感染へと症状が段階的に増悪していき、治療抵抗性となる。一方、Ph+ ALLは小児及び高齢者にみられ、初期治療後に再発する、あるいは治療抵抗性の患者の予後は極めて不良である。
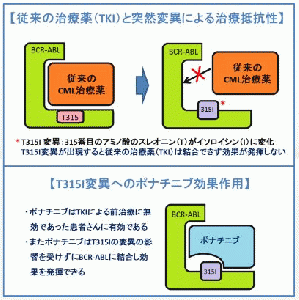
CMLやPh+ ALLの治療薬には、第一選択薬としてTKIが使用されるが、病気の進行によりTKI治療の抵抗性を示すようになり、十分な治療効果が得られない場合がある。また、副作用によりTKIの治療を継続できない不耐容の患者も存在する。
「ポナチニブ」
「ポナチニブ」は、アリアド社が創製したCMLやPh+ ALLに発現するBCR-ABLに作用するTKIであり、新規に化学合成された経口TKIで、野生型BCR-ABL及び他のTKIに抵抗性を示す変異型BCR-ABLであるT315I変異などに対して、阻害作用を示すように設計されている。「ポナチニブ」は、欧米では既に販売開始され、既存の治療薬に抵抗性又は不耐容の慢性骨髄性白血病やフィラデルフィア染色体陽性急性リンパ性白血病の患者に使用されており、日本を含めたアジアで要望されている。
(画像はニュースリリースより)
大塚製薬株式会社 ニュースリリース
http://www.otsuka.co.jp/company/release/
-->