- TOP
- >
- ノバルティス、「タシグナ(R)」が小児の慢性骨髄性白血病治療薬として承認を取得と発表
新着ニュース30件
2017年12月26日 22:00
血液腫瘍領域における経験とリーダーシップで貢献する
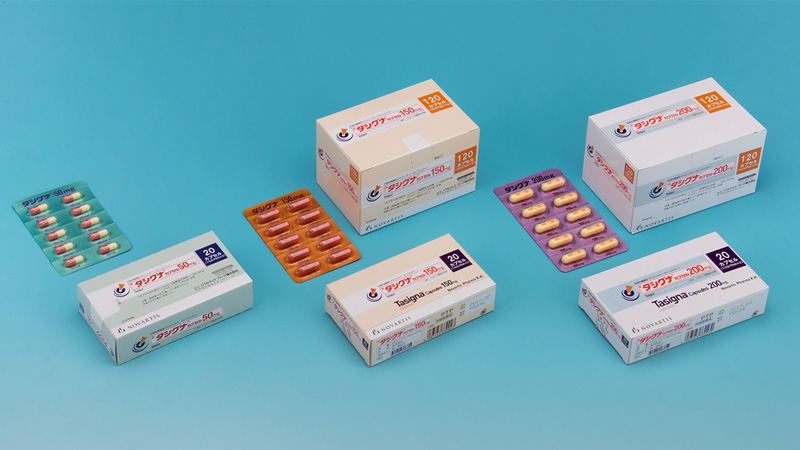
ノバルティスファーマ株式会社は2017年12月25日のプレスリリースで、「タシグナ(R)カプセル50mg・150mg・200mg」(一般名:ニロチニブ塩酸塩水和物)について、慢性期又は移行期の慢性骨髄性白血病(CML)を効能又は効果として、小児に対する用法および用量に関する製造販売承認事項一部変更承認を取得したと発表した。また、2017年11月29日に薬価収載された「タシグナ」の新剤形である50mgカプセルを、2017年12月25日付けで発売することも合わせて発表した。
チロシンキナーゼを阻害し効果を発揮
CMLの標準治療は、国内外ともにチロシンキナーゼ阻害薬(TKI)による治療であるが、国内で承認されているTKIはいずれも小児のCMLに対する適応を有していなかったことから、CMLの小児患者に対する「タシグナ」の至適用法・用量の検討を目的として開発したとノバルティスは述べている。今回の承認は、初発もしくはイマチニブ又はダサニチブに抵抗性又は不耐容の慢性期CMLの小児患者58例(日本人9例を含む)を対象にした国際共同第2相試験に基づいており、初発の慢性期CML小児患者のうち、主要評価項目であるサイクル12時点までに少なくとも1回分子遺伝学的効果(MMR)が得られた割合は、25例中16例の64.0%であった。
(画像はプレスリリースより)
ノバルティスファーマ株式会社プレスリリース
https://www.novartis.co.jp/news/media-releases/
ノバルティスファーマ株式会社
https://www.novartis.co.jp/
-->