- TOP
- >
- ジャパンワクチン、皮内投与型季節性インフルエンザワクチンの国内製造販売承認を申請
新着ニュース30件
2015年4月15日 15:00
4社共同で開発
第一三共株式会社(以下、第一三共)とテルモ株式会社(以下、テルモ)は、第一三共の関連会社であるジャパンワクチン株式会社(以下、ジャパンワクチン)が、皮内投与型季節性インフルエンザワクチンの国内製造販売承認申請を行ったと発表した。同ワクチンは、第一三共とテルモの皮内投与型感染症予防ワクチンの実用化に関する2012年2月23日付に締結された基本合意にもとづき、第一三共、テルモ、ジャパンワクチン、第一三共のグループ会社である北里第一三共ワクチン株式会社(以下、北里第一三共)の4社共同で開発したプレフィルドシリンジ型の皮内用インフルエンザHAワクチン。
テルモが開発した皮内投与専用の注射針とプレフィルドシリンジを組み合わせた皮内投与型デバイスに、北里第一三共のインフルエンザHAワクチンが充填されたものとなっている。
皮内注射
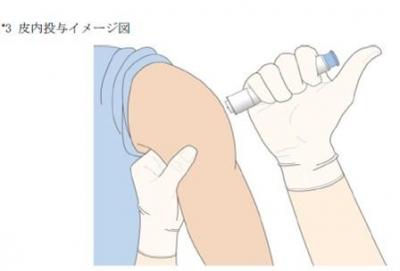
皮内注射は、皮内など皮膚上層部に注射することで、免疫システムによる抗原認識を効率的に強化でき、従来の皮下や筋肉に注射するよりもワクチンの効果を高めるとされている。テルモは、皮内注射を簡便かつ確実に実施できることをコンセプトとした皮下組織の末梢血管及び神経に対するリスク低減できるように、注射針を短くするといった工夫を施した皮内投与型デバイスを開発。
同シリンジは、従来は困難であった皮内注射を簡便かつ確実に行うことを可能とするだけでなく、針に対する抵抗感のような負担軽減も期待されている。
従来の皮下注射製剤と同等以上の免疫原性を確認
同ワクチンの免疫原性及び安全性を評価するための第3相臨床試験では、試験した全てのインフルエンザウイルス株に対して従来の皮下注射製剤と比較して同等以上の免疫原性が確認されている。また、これまで実施した臨床試験においても良好な安全性が確認されている。(画像はニュースリリースより)
第一三共株式会社 ニュースリリース
http://www.daiichisankyo.co.jp/news/detail/006265.html
テルモ株式会社
http://www.terumo.co.jp/
-->