- TOP
- >
- Aドメインの基質特異性設計が可能に 高感度ELISA法
新着ニュース30件
2015年10月24日 11:30
創薬シーズ開発加速に期待
京都大学、掛谷秀昭薬学研究科教授、石川文洋同特定助教らは、ペプチド性天然化合物の合成酵素である非リボソーム性ペプチド合成酵素のアデニレーション(A)ドメインを標的とする、合成小分子プローブ群を創出し、その固定化により、Aドメインの基質特異性を迅速、簡便、かつ高感度に検出可能なELISA法を開発したと発表した。背景
近年、微生物が産生するペプチド性天然有機化合物の酵素システムを人為的に改変し、非天然化合物を創出する試みが多数報告されている。その理由は微生物が産生するペプチド性天然有機化合物の構造上多様性や強力な生物活性を有するためであり、研究ツールとなり創薬シーズとなっているからである。しかし、タンパク質工学的手法が成熟しつつある今日においても非天然化合物の創出は容易ではない。一因として、Aドメイン変異体ライブラリーから、望む基質特異性を有するAドメインを迅速に選別する手法が、確立されていない点が挙げられる。
研究成果
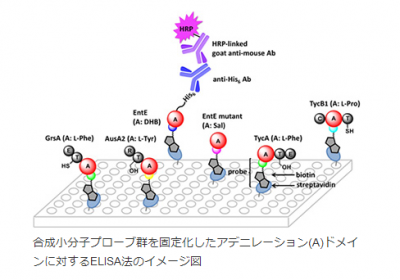
今回の研究では、抗生物質グラミシジンSの生合成に関与するNRPS(GrsA)、抗生物質チロシジンの生合成に関与するNRPS(TycA、TycB1)、タンパク質分解酵素カルパイン阻害剤アウレウシミンの生合成に関与するNRPS(AusA2)、鉄キレーター(シデロフォア)エンテロバクチンの生合成に関与するNRPS(EntE)のAドメインを標的タンパク質とした。まず、Aドメインに高い親和性を有するアミノアシル-AMS-ビオチンを創製し、これら化合物のビオチン官能基を利用し、ストレプトアビジンを吸着したプレートにプローブ群を固定化した、Aドメインに対するELISA法の構築を行った。
これにより、Aドメイン変異体ライブラリーから設計した酵素機能を有する、Aドメインを取得するための基盤技術が構築できた。
今回の研究により、自由自在にAドメインの基質特異性を設計が可能になると共に、非天然化合物の創出や複雑天然化合物の誘導体化が可能になり、創薬シーズ開発の加速が期待される。
(画像は京都大学・研究成果より)
京都大学 研究成果
http://www.kyoto-u.ac.jp/ja/research/research_results/2015/
-->